Йод, свойства атома, химические и физические свойства.
I 53 Йод
126,90447(3) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p5
Йод — элемент периодической системы химических элементов Д. И. Менделеева с атомным номером 53. Расположен в 17-й группе (по старой классификации — главной подгруппе седьмой группы), пятом периоде периодической системы.
Атом и молекула йода. Формула йода. Строение атома йода
Свойства йода (таблица): температура, плотность, давление и пр.
Физические свойства йода
Химические свойства йода. Взаимодействие йода. Химические реакции с йодом
Таблица химических элементов Д.И. Менделеева
Атом и молекула йода. Формула йода. Строение атома йода:
Йод (лат. Iodum, от греч. ἰώδης — «фиалковый (фиолетовый)») – химический элемент периодической системы химических элементов Д. И. Менделеева с обозначением I и атомным номером 53. Расположен в 17-й группе (по старой классификации – главной подгруппе седьмой группы), пятом периоде периодической системы.
Йод – неметалл. Относится к группе галогенов.
Йод обозначается символом I.
Как простое вещество йод при нормальных условиях представляет собой кристаллы чёрно-серого цвета с фиолетовым металлическим блеском. Йод легко образует фиолетовые пары, обладающие резким запахом.
Молекула йода двухатомна.
Химическая формула йода I2.
Электронная конфигурация атома йода 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p5. Потенциал ионизации (первый электрон) атома йода равен 1008,39 кДж/моль (10,451260(25) эВ).
Строение атома йода. Атом йода состоит из положительно заряженного ядра (+53), вокруг которого по пяти оболочкам движутся 53 электрона. При этом 46 электронов находятся на внутреннем уровне, а 6 электронов – на внешнем. Поскольку йод расположен в пятом периоде, оболочек всего пять. Первая – внутренняя оболочка представлена s-орбиталью. Вторая – внутренняя оболочка представлены s- и р-орбиталями. Третья и четвертая – внутренние оболочки представлены s-, р- и d-орбиталями. Пятая – внешняя оболочка представлена s- и р-орбиталями. На внешнем энергетическом уровне атома йода на 5s-орбитали находятся два спаренных электрона, на 5p-орбитали – четыре спаренных и один неспаренный электрон. В свою очередь ядро атома йода состоит из 53 протонов и 74 нейтронов. Йод относится к элементам p-семейства.
Радиус атома йода (вычисленный) составляет 115 пм.
Атомная масса атома йода составляет 126,90447(3) а. е. м.
Йод – химически активный неметалл.
Изотопы и модификации йода:
Свойства йода (таблица): температура, плотность, давление и пр.:
Подробные сведения на сайте ChemicalStudy.ru
| 100 | Общие сведения | |
| 101 | Название | Йод |
| 102 | Прежнее название | |
| 103 | Латинское название | Iodum |
| 104 | Английское название | Iodine |
| 105 | Символ | I |
| 106 | Атомный номер (номер в таблице) | 53 |
| 107 | Тип | Неметалл |
| 108 | Группа | Галоген |
| 109 | Открыт | Бернар Куртуа, Франция, 1811 г. |
| 110 | Год открытия | 1811 г. |
| 111 | Внешний вид и пр. | Кристаллы чёрно-серого цвета с фиолетовым металлическим блеском. Легко образует фиолетовые пары, обладающие резким запахом |
| 112 | Происхождение | Природный материал |
| 113 | Модификации | |
| 114 | Аллотропные модификации | |
| 115 | Температура и иные условия перехода аллотропных модификаций друг в друга | |
| 116 | Конденсат Бозе-Эйнштейна | |
| 117 | Двумерные материалы | |
| 118 | Содержание в атмосфере и воздухе (по массе) | 0 % |
| 119 | Содержание в земной коре (по массе) | 0,000049 % |
| 120 | Содержание в морях и океанах (по массе) | 6,0·10-6 % |
| 121 | Содержание во Вселенной и космосе (по массе) | 1,0·10-7 % |
| 122 | Содержание в Солнце (по массе) | |
| 123 | Содержание в метеоритах (по массе) | 0,000025 % |
| 124 | Содержание в организме человека (по массе) | 0,00002 % |
| 200 | Свойства атома | |
| 201 | Атомная масса (молярная масса) | 126,90447(3) а. е. м. (г/моль) |
| 202 | Электронная конфигурация | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p5 |
| 203 | Электронная оболочка | K2 L8 M18 N18 O7 P0 Q0 R0
|
| 204 | Радиус атома (вычисленный) | 115 пм |
| 205 | Эмпирический радиус атома* | 140 пм |
| 206 | Ковалентный радиус* | 139 пм |
| 207 | Радиус иона (кристаллический) | I–
206 (6) пм, I 5+ 109 (6) пм, I 7+ 67 (6) пм (в скобках указано координационное число – характеристика, которая определяет число ближайших частиц (ионов или атомов) в молекуле или кристалле) |
| 208 | Радиус Ван-дер-Ваальса | 198 пм |
| 209 | Электроны, Протоны, Нейтроны | 53 электрона, 53 протона, 74 нейтронов |
| 210 | Семейство (блок) | элемент p-семейства |
| 211 | Период в периодической таблице | 5 |
| 212 | Группа в периодической таблице | 17-ая группа (по старой классификации – главная подгруппа 7-ой группы) |
| 213 | Эмиссионный спектр излучения | |
| 300 | Химические свойства | |
| 301 | Степени окисления | -1, 0, +1, +2, +3, +4, +5, +6, +7 |
| 302 | Валентность | I, III, V, VII |
| 303 | Электроотрицательность | 2,66 (шкала Полинга) |
| 304 | Энергия ионизации (первый электрон) | 1008,39 кДж/моль (10,451260(25) эВ) |
| 305 | Электродный потенциал | I2 + 2e– → 2I–, Eo = +0,536,
I3– + 2e– → 3I–, Eo = +0,545 |
| 306 | Энергия сродства атома к электрону | 295,1531(4) кДж/моль (3,0590465(37) эВ) – йод 127I,
295,154(4) кДж/моль (3,059052(38) эВ) – йод 128I |
| 400 | Физические свойства | |
| 401 | Плотность* | 4,933 г/см3 (при 20 °C и иных стандартных условиях, состояние вещества – твердое тело)
4,866 г/см3 (при 60 °C и иных стандартных условиях, состояние вещества – твердое тело) |
| 402 | Температура плавления* | 113,7 °C (386,85 K, 236,66 °F) |
| 403 | Температура кипения* | 184,3 °C (457,4 K, 363,7 °F) |
| 404 | Температура сублимации* | При нагревании при атмосферном давлении |
| 405 | Температура разложения | |
| 406 | Температура самовоспламенения смеси газа с воздухом | |
| 407 | Удельная теплота плавления (энтальпия плавления ΔHпл) | 15,52 кДж/моль |
| 408 | Удельная теплота испарения (энтальпия кипения ΔHкип)* | 41,57 кДж/моль |
| 409 | Удельная теплоемкость при постоянном давлении | |
| 410 | Молярная теплоёмкость | 54,44 Дж/(K·моль) |
| 411 | Молярный объём | 25,689 см³/моль |
| 412 | Теплопроводность | 0,449 Вт/(м·К) (при стандартных условиях),
0,45 Вт/(м·К) (при 300 K) |
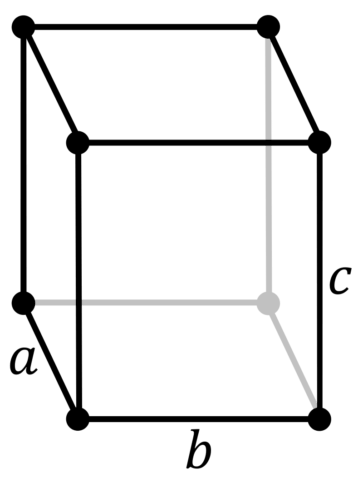
| 500 | Кристаллическая решётка | |
| 511 | Кристаллическая решётка #1 | |
| 512 | Структура решётки | Орторомбическая
|
| 513 | Параметры решётки | a = 7,18 Å, b = 4,71 Å, c = 9,81 Å |
| 514 | Отношение c/a | |
| 515 | Температура Дебая | |
| 516 | Название пространственной группы симметрии | Cmca |
| 517 | Номер пространственной группы симметрии | 64 |
| 900 | Дополнительные сведения | |
| 901 | Номер CAS | 7553-56-2 |
Примечание:
205* Эмпирический радиус атома йода согласно [3] составляет 136 пм.
206* Ковалентный радиус йода согласно [1] и [3] составляет 139±3 пм и 133 пм соответственно.
401* Плотность йода согласно [3] и [4] составляет 4,93 г/см3 (при 25 °C и иных стандартных условиях, состояние вещества – твердое тело) и 4,94 г/см3 (при 20 °C и иных стандартных условиях, состояние вещества – твердое тело) соответственно.
402* Температура плавления йода согласно [3] и [4] составляет 113,5 °С (386,65 K, 236,3 °F) и 114 °С (387,15 K, 237,2 °F) соответственно. Жидкий йод согласно [3] можно получить, нагревая его под давлением.
403* Температура кипения йода согласно [3] и [4] составляет 184,35 °C (457,5 K, 363,83 °F) и 185,5 °С (458,65 K, 365,9 °F) соответственно.
408* Удельная теплота испарения (энтальпия кипения ΔHкип) йода согласно [3] составляет 41,95 кДж/моль.
Физические свойства йода:
Химические свойства йода. Взаимодействие йода. Химические реакции с йодом:
Получение йода:
Применение йода:
Таблица химических элементов Д.И. Менделеева
- 1. Водород
- 2. Гелий
- 3. Литий
- 4. Бериллий
- 5. Бор
- 6. Углерод
- 7. Азот
- 8. Кислород
- 9. Фтор
- 10. Неон
- 11. Натрий
- 12. Магний
- 13. Алюминий
- 14. Кремний
- 15. Фосфор
- 16. Сера
- 17. Хлор
- 18. Аргон
- 19. Калий
- 20. Кальций
- 21. Скандий
- 22. Титан
- 23. Ванадий
- 24. Хром
- 25. Марганец
- 26. Железо
- 27. Кобальт
- 28. Никель
- 29. Медь
- 30. Цинк
- 31. Галлий
- 32. Германий
- 33. Мышьяк
- 34. Селен
- 35. Бром
- 36. Криптон
- 37. Рубидий
- 38. Стронций
- 39. Иттрий
- 40. Цирконий
- 41. Ниобий
- 42. Молибден
- 43. Технеций
- 44. Рутений
- 45. Родий
- 46. Палладий
- 47. Серебро
- 48. Кадмий
- 49. Индий
- 50. Олово
- 51. Сурьма
- 52. Теллур
- 53. Йод
- 54. Ксенон
- 55. Цезий
- 56. Барий
- 57. Лантан
- 58. Церий
- 59. Празеодим
- 60. Неодим
- 61. Прометий
- 62. Самарий
- 63. Европий
- 64. Гадолиний
- 65. Тербий
- 66. Диспрозий
- 67. Гольмий
- 68. Эрбий
- 69. Тулий
- 70. Иттербий
- 71. Лютеций
- 72. Гафний
- 73. Тантал
- 74. Вольфрам
- 75. Рений
- 76. Осмий
- 77. Иридий
- 78. Платина
- 79. Золото
- 80. Ртуть
- 81. Таллий
- 82. Свинец
- 83. Висмут
- 84. Полоний
- 85. Астат
- 86. Радон
- 87. Франций
- 88. Радий
- 89. Актиний
- 90. Торий
- 91. Протактиний
- 92. Уран
- 93. Нептуний
- 94. Плутоний
- 95. Америций
- 96. Кюрий
- 97. Берклий
- 98. Калифорний
- 99. Эйнштейний
- 100. Фермий
- 101. Менделеевий
- 102. Нобелий
- 103. Лоуренсий
- 104. Резерфордий
- 105. Дубний
- 106. Сиборгий
- 107. Борий
- 108. Хассий
- 109. Мейтнерий
- 110. Дармштадтий
- 111. Рентгений
- 112. Коперниций
- 113. Нихоний
- 114. Флеровий
- 115. Московий
- 116. Ливерморий
- 117. Теннессин
- 118. Оганесон
Таблица химических элементов Д.И. Менделеева
Источники:
- https://en.wikipedia.org/wiki/Iodine
- https://de.wikipedia.org/wiki/Iod
- https://ru.wikipedia.org/wiki/Иод
- http://chemister.ru/Database/properties.php?dbid=1&id=263
- https://chemicalstudy.ru/yod-svoystva-atoma-himicheskie-i-fizicheskie-svoystva/
Примечание: © Фото https://www.pexels.com, https://pixabay.com
йод атомная масса степень окисления валентность плотность температура кипения плавления физические химические свойства структура теплопроводность электропроводность кристаллическая решетка
атом нарисовать строение число протонов в ядре строение электронных оболочек электронная формула конфигурация схема строения электронной оболочки заряд ядра состав масса орбита уровни модель радиус энергия электрона переход скорость спектр длина волны молекулярная масса объем атома
электронные формулы сколько атомов в молекуле йода йод
сколько электронов в атоме свойства металлические неметаллические термодинамические